Minerai d'uranium extrait à Lodève, France (©photo)
À RETENIR
- L'uranium naturel est un métal lourd assez commun sur Terre.
- Il est constitué de 3 isotopes : l'uranium 238 (99,28%), l'uranium 235 (0,71%, atome fissile dont la teneur est enrichie pour produire de l'électricité) et des traces d’uranium 234.
- Presque 70% de la production mondiale d'uranium naturel provient de 3 pays : le Kazakhstan, le Canada et la Namibie.
Définition
L'uranium est un métal gris argenté, le plus lourd présent naturellement sur Terre. Cet élément chimique porte le numéro atomique 92 et n’est constitué que de trois isotopes :
- l'uranium 238, le plus lourd des atomes présent dans l’écorce terrestre, le plus stable des trois et donc le plus abondant (99,28%) ;
- l'uranium 235 (0,71%), seul atome naturel fissile ;
- enfin des traces d’uranium 234 (0,006%).
Présence sur Terre et en mer
L'uranium est un élément naturel assez commun : il est plus abondant que l'argent ou l'or et se trouve partout dans l'écorce terrestre, surtout dans les terrains granitiques ou sédimentaires, à des teneurs moyennes d'environ 3 g d'uranium / tonne. Ainsi, le sous-sol d'un jardin de 400m2 peut contenir, sur une profondeur de 10 m environ, 24 kg d'uranium. On trouve de l'uranium en quantité importante dans les profondeurs de la Terre où il est, avec le thorium et le potassium, un élément déterminant de la géothermie de notre planète, donc de son volcanisme et de sa sismicité. En outre, il est environ deux fois et demi plus dense que le fer.
Enfin, l'eau de mer contient environ 3 mg d'uranium / m3, ce qui représente à l'échelle mondiale environ 4,5 milliards de tonnes d'uranium dissoutes dans les océans.
Radioactivité
L'uranium est radioactif. Cela signifie que les noyaux de ses atomes sont trop lourds pour être stables dans le temps. Ils se transforment spontanément en d’autres éléments radioactifs plus légers (par exemple, l'uranium 238 en thorium 234) qui à leur tour disparaîtront par décroissance radioactive.
Ce n’est qu’après une douzaine de désintégrations successives que la chaîne radioactive aboutit à un isotope stable du plomb (plomb 206 dans le cas de la chaîne de décroissance de l’uranium 238). Mais les isotopes de l’uranium naturel ont des périodes de désintégration très longue : 4,5 milliards d'années pour l'uranium 238, 700 millions d'années pour l'uranium 235. Cela explique qu’ils soient encore présents à l’état naturel sur Terre et cela fait de l’uranium naturel un élément peu radioactif. Notons cependant qu’un des descendants de l’uranium dans les chaînes de décroissance radioactive est le radon dont la radioactivité n’est pas négligeable et qui, étant gazeux, passe dans l’air lorsque l’uranium est extrait.
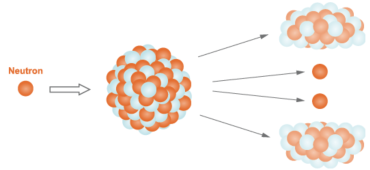
L’uranium 235 est le seul isotope naturel fissile, c'est-à-dire susceptible de se fragmenter, spontanément ou par capture d’un neutron, en deux atomes de masses proches avec émission de plusieurs neutrons et d'un rayonnement gamma intense. L’uranium 238, beaucoup plus stable et très peu fissile, est dit fertilecar il peut être transformé, par absorption d'un neutron, en plutonium 239 (encore plus fissile que l'uranium 235).
Usages nucléaires
C’est cette aptitude directe ou indirecte à la fission qui fait de l’uranium naturel la principale matière première utilisée aujourd’hui par l’industrie nucléaire pour produire de l’électricité, propulser des navires, fabriquer des armes de très grande puissance mais aussi synthétiser des radioisotopes pour l’imagerie médicale, la radiothérapie et l’industrie.
Dans les réacteurs nucléaires, de l’uranium « enrichi » en isotope 235 (généralement à des taux de 3 à 5%) est utilisé. Cet uranium enrichi permet de produire plus de 9% de l’électricité générée chaque année dans le monde.
Exploitation : extraction et transformation
L'uranium naturel est un métal que l'on peut extraire par plusieurs techniques. En règle générale, le minerai existant est à faible teneur en uranium (quelques kg par tonne de minerai) mais peut exceptionnellement atteindre des teneurs beaucoup plus élevées (par exemple au Canada ou au Niger). Les coûts de transport encouragent une étape de concentration du composé sur place.
Le processus d'enrichissement :
- Par des méthodes chimiques, on transforme le minerai en « yellowcake » qui contient environ 750 kg d’uranium par tonne ;
- Le yellowcake est ensuite purifié puis oxydé en oxyde d'uranium (U3O8) ;
- On le transforme ensuite en hexafluorure d’uranium (UF6) ;
- Pour pouvoir l’enrichir en uranium 235 (en passant la proportion de cet isotope de 0,7% à 3-5%) par diffusion gazeuse ou centrifugation sélective.
L’uranium enrichi est alors utilisable au sein de barre de combustible dans les centrales électronucléaires. Les applications militaires requièrent des enrichissements beaucoup plus élevés (> 80%).
L’uranium enrichi est utilisé dans près de 420 réacteurs à travers le monde. En France, 57 réacteurs nucléaires (en incluant l'EPR de Flamanville) produisent près des deux tiers de l’électricité nationale (67,4% en 2024 selon les dernières données de RTE). Aux États-Unis, une centaine de réacteurs produisent un peu moins d'un cinquième de l'électricité américaine.
Où trouve-t-on de l'uranium sur Terre ?
La production mondiale d'uranium naturel atteint près de 49 355 tonnes en 2022, selon la Word Nuclear Association qui promeut les activités de la filière(1).
Pays produisant le plus d'uranium naturel
Les 10 principaux pays producteurs d'uranium naturel sont :
- le Kazakhstan (21 227 tonnes extraites en 2022, soit 43% du total mondial) ;
- le Canada (7 351 tonnes, 14,9%) ;
- la Namibie (5 613 t, 11,4%) ;
- l'Australie (4 553 t, 9,2%) ;
- l'Ouzbékistan (estimation de 3 300 t, 6,7%) ;
- la Russie (2 508 t, 5,1%) ;
- le Niger (2 020 t, 4,1%) ;
- la Chine (estimation de 1 700 t, 3,4%) ;
- l'Inde (estimation de 600 t, 1,2%) ;
- l'Afrique du Sud (estimation de 200 t, 0,4%).
Les principales compagnies gérant l'extraction d'uranium naturel sont Kazatomprom (23% de la production mondiale en 2022), Cameco (12%) et Orano (11%).
Il y a eu en France plus de 200 sites d'extraction et de traitement de minerai d'uranium qui ont été progressivement fermés. L'essentiel de l'uranium français provient historiquement des mines d'Arlit au Niger, gérées par Orano.
Les réserves mondiales d'uranium récupérables à moins de 260 $/lb (seuil de rentabilité économique en 2019, contre 40 $ en 2010) atteindraient 8 millions de tonnes, soit trois fois plus que dix ans auparavant. Selon la World Nuclear Association, cela permettrait de satisfaire la demande mondiale actuelle supposée stable pendant plus d'un siècle.
Rappelons que la consommation d'énergie nucléaire compte pour moins de 6% de la consommation mondiale d’énergie primaire, contre plus de 80% pour les sources fossiles (pétrole, charbon, gaz). Cette part est susceptible d'augmenter à l'échelle mondiale en cas de diminution de la production à partir d'énergies fossiles.
Le développement de réacteurs de 4e génération utilisant la totalité de l’uranium et ne nécessitant pas d’enrichissement permettrait de porter les réserves disponibles à plusieurs millénaires, ce qui ferait du nucléaire une énergie durable et sans effet de serre, selon ses partisans.
Découverte de l'uranium
L'uranium a été mis en évidence en 1789 par le chimiste prussien Martin Heinrich Klaproth en examinant un morceau de roche provenant de Jáchymov, ville de l'actuelle République tchèque. Il lui donna le nom de « urane » ou « uranite » en référence à la découverte de la planète Uranus 8 ans plus tôt par William Herschel.
Le chimiste français Eugène-Melchior Péligot établit que la roche analysée par Klaproth est en réalité composée de deux atomes d'oxygène et d'un atome de métal qu'il appela « uranium ».
La radioactivité de l'uranium ne fut découverte qu'en 1896 par Henri Becquerel lorsqu'il constata que des plaques photographiques placées à côté d'échantillons d'uranium avaient été noircies alors qu'elles n'avaient jamais été exposées à la lumière. Becquerel découvrit ainsi le phénomène de radioactivité et poursuivit son étude entre autre avec les époux Curie.
À l'origine, le minerai d'uranium était utilisé dans la céramique pour ses pigments jaunes, oranges et verts. Ce n'est qu'avec la découverte de la radioactivité que les premières applications médicales ont émergé. Le projet Manhattan a marqué le début de son utilisation à des fins militaires qui se sont poursuivies tout au long de la guerre froide. Aujourd'hui, les applications dans le nucléaire civil destiné à la production d'électricité et à la médecine sont prépondérantes.
Des conséquences environnementales à maîtriser
L'uranium terrestre est faiblement radioactif et ne présente pas de danger, tant qu’il reste dans son état naturel. Ainsi, l'eau (douce ou salée) et les légumes qui nous mangeons contiennent naturellement de faibles quantités d'uranium et aucun impact sur la santé n'a jamais été prouvé.
Environ 98% de l'uranium pénétrant dans l'organisme n'est pas absorbé et est évacué par les voies naturelles.
Il peut en être autrement de l'uranium extrait de la mine. En effet, les différentes étapes de son extraction puis de sa concentration pour obtenir du yellowcake supposent un contrôle strict :
- des rejets atmosphériques, en particulier de radon, gaz radioactif occlus dans le minerai, et des poussières de minerai, peuvent provoquer des cancers du poumon ;
- des rejets liquides ou solides (pour éviter qu’ils polluent les nappes phréatiques, les eaux de boisson ne devant pas contenir plus de 15 mg d'uranium par litre d'eau).
La toxicité de l'uranium est de deux types :
- la toxicité chimique de l’uranium est la même que celle des autres métaux lourds comme le plomb ou le mercure : les reins sont les organes critiques. Les atteintes peuvent être graves (saturnisme, encéphalopathie) ;
- la toxicité radiologique de l’uranium naturel est nettement (40 fois) plus faible que sa toxicité chimique car il est peu radioactif. En réalité, tout dépend de l’intensité et de la durée d’exposition aux radiations.
Exposition à la radioactivité naturelle
Dans notre environnement, nous sommes exposés en moyenne à des radiations de 3,5 à 4 mSv/an(2) en France, dont environ 2,5 mSv/an en raison de la radioactivité naturelle et 1,1 mSv/an d'origine médicale, le seuil à ne pas dépasser étant fixé à 4,7 mSv/an et la radioactivité artificielle complémentaire induite par les activités humaines étant en France (2010) d’environ 0,06 mSv/an (maximum autorisé : 1 mSv/an). Un ensemble complet de normes sanitaires existe à l'échelle nationale et internationale (OMS).
L’exposition à la radioactivité naturelle e, France est due pour l’essentiel au radon 222, gaz rare issu de la séquence de désintégration de l’uranium 238 qui passe par le thorium 234 puis le radium 226.
Ce niveau d’exposition est faible. Dans certaines parties de l’Inde, de la Chine ou du Brésil, l’exposition naturelle atteint 20 fois la moyenne française, sans dommage avéré pour les populations.
En ce qui concerne l’uranium, l’avenir semble être à une plus grande vigilance sur ses conditions d’extraction, de manipulation et de transport, comme sur celles de tous les métaux lourds pour en limiter strictement l’impact sur l’environnement.
Un uranium toujours plus demandé et toujours plus cher
Lorsque les stocks prouvés d'uranium à très haute teneur sont insuffisants pour faire face à la demande, les cours de l'uranium sont en hausse. Cette situation a donné un regain d'intérêt à la prospection minière ces dernières années et d'anciens gisements sont actuellement réouverts.
La demande en uranium connaît un pic dans les années 1950 pendant la course aux armements entre les États-Unis et l'URSS. Elle reprend dans les années 1970 avec le démarrage du nucléaire civil. Elle se stabilise au début des années 1980 lorsque la plupart des centrales sont construites. La pression des groupes d'opinion antinucléaires accentue cette tendance dès 1986 après la catastrophe de Tchernobyl.
Le prix de la livre d'uranium (à peu près 453 grammes), de 43$ en 1978, tombe alors à 33$ en 1981 et atteint son minimum historique à 7$ en 2001.
Le moratoire sur la construction de nouvelles centrales nucléaires, imposé de fait en 1986 (Tchernobyl), prend fin avec le protocole de Kyoto qui réhabilite le nucléaire comme une énergie « carbon free ».
Dans ce contexte plus porteur avec un nucléaire alors réputé compétitif d'un point de vue économique, le cours de l'uranium sur les marchés spot remonte au-dessus de 120$/lb en 2007. L’accident de Fukushima en mars 2011 ouvre une nouvelle période d’incertitudes avec toutefois une pression accrue de la demande énergétique des pays émergents.
En janvier 2024, le prix de la livre d'uranium a dépassé la barre symbolique des 100$(3). En l'espace d'un an, les prix du combustible nucléaire ont plus que doublé en raison des programmes de construction de réacteurs et des problèmes de production rencontrés par les principaux acteurs miniers. Cependant, cela ne devrait pas compromettre la rentabilité de l'énergie nucléaire.
L'augmentation du prix des énergies fossiles est une tendance lourde sur plusieurs décennies renforcée, à laquelle s'ajoute la prise en compte du changement climatique et de la nécessaire réduction des émissions de gaz à effet de serre. Les États cherchent des alternatives au charbon, au pétrole et au gaz naturel (bien que l'émergence des hydrocarbures non conventionnels bouleversent cette tendance dans certaines zones).
L'énergie nucléaire, par sa densité un million de fois supérieure aux énergies fossiles, fait que de nombreux pays la choisissent pour des raisons économiques ou stratégiques - comme la France. Mais cette densité est intrinsèquement porteuse de risques comme les accidents nucléaires le rappellent. Elle exige une sûreté exceptionnelle qui doit encore être améliorée.
Actuellement, le monde dispose de 417 réacteurs nucléaires opérationnels selon l'AIE (auxquels s'ajoute une soixantaine de réacteurs supplémentaires en cours de construction). Simultanément l’effort de développement des réacteurs de 4e génération s’intensifie dans le monde, en particulier en Chine et en Inde, pour s’affranchir des contraintes attachées à l’emploi d’un uranium 235 se raréfiant et passer, avec l’uranium 238, à l’ère du nucléaire « fertile et abondant ».