Thorium utilisé au Bhabha Atomic Research Centre à Mumbai en Inde.
Le thorium est un métal très lourd de couleur argentée qui se trouve naturellement et abondamment dans la croûte terrestre, souvent associé à d'autres minéraux radioactifs.
Il est principalement étudié pour son potentiel en tant que combustible nucléaire, en raison de son abondance et de sa capacité à produire de l'énergie sans générer autant de déchets à longue durée de vie que l'uranium. Le thorium est ainsi considéré comme une alternative plus sûre et plus durable pour l'énergie nucléaire.
Origine et numéro atomique
Le thorium a été identifié en 1829 par le chimiste suédois Jöns Jacob Berzelius, après avoir été extrait sous forme de minerai dans l'île de Løvøya en Norvège. Le nom de ce minerai provient du dieu du tonnerre dans la mythologie nordique, Thor.
La radioactivité du thorium a été découverte en 1898 par la physicienne Marie Curie et par le chimiste Gerhard Carl Schmidt.
Le thorium se situe en fin du tableau de Mendeleïev (numéro atomique = 90) dans la famille des actinides, tout comme l’uranium naturel (Z = 92)(1). Il dispose d’un seul isotope : le thorium 232.
Usages et intérêts
Le thorium possède des qualités physico-chimiques exceptionnelles : il ne fond qu’à 1 750°C et se vaporise vers 4 800°C (Pa). Il a de nombreuses applications industrielles comme matériau réfractaire, cathode en électronique, catalyseur en chimie, pour le cracking du pétrole, etc.
Une voie prometteuse pour le thorium comme combustible nucléaire semble être celle l'utilisation du mélange thorium-uranium sous la forme de sel fluorés fondus, servant à la fois de combustible et de caloporteur dans un réacteur à sel fondus (RSF). La filière thorium-uranium 233 avait déjà suscité l’intérêt des chercheurs dès les années 1950. Elle avait alors été rejetée, au bénéfice de la filière uranium-plutonium car les conditions de radioprotection n’étaient alors pas maîtrisées.
Le thorium peut également être utilisé par des réacteurs de cette nouvelle génération dans des surgénérateurs à neutrons rapides.
Différences avec l'uranium
Le thorium est 3 à 4 plus abondant que l’uranium naturel (voir pargraphe sur les ressources plus bas dans l'article) et est très faiblement radioactif (demi-vie de 14 milliards d’années).
Le thorium n'est pas fissile (l’uranium est le seul élément naturel à comporter un isotope fissile (uranium 235). mais fertile, c'est-à-dire qu’il et peut se transformer par absorption d’un neutron en uranium 233, élément fissile tout comme l’uranium 235 utilisé dans les réacteurs actuels à eau pressurisée (type des réacteurs du parc nucléaire français). Or, la fission de l’uranium 233 produit un peu plus de neutrons que celle de l’uranium 235, ce qui permettrait de produire davantage d’énergie avec une quantité donnée de minerai.
Dans le cas de l'uranium, la réaction en chaîne est donc amorcée par de l'uranium 235 présent dans le minerai naturel puis dans le combustible préparé à partir de ce minerai. Dans le cas du thorium, « il faut ajouter artificiellement un élément fissile (ici de l'uranium 235) dans le combustible préparé à partir de minerai naturel de thorium qui est non fissile », explique le CEA(2) (comme l'illustre son schéma suivant).
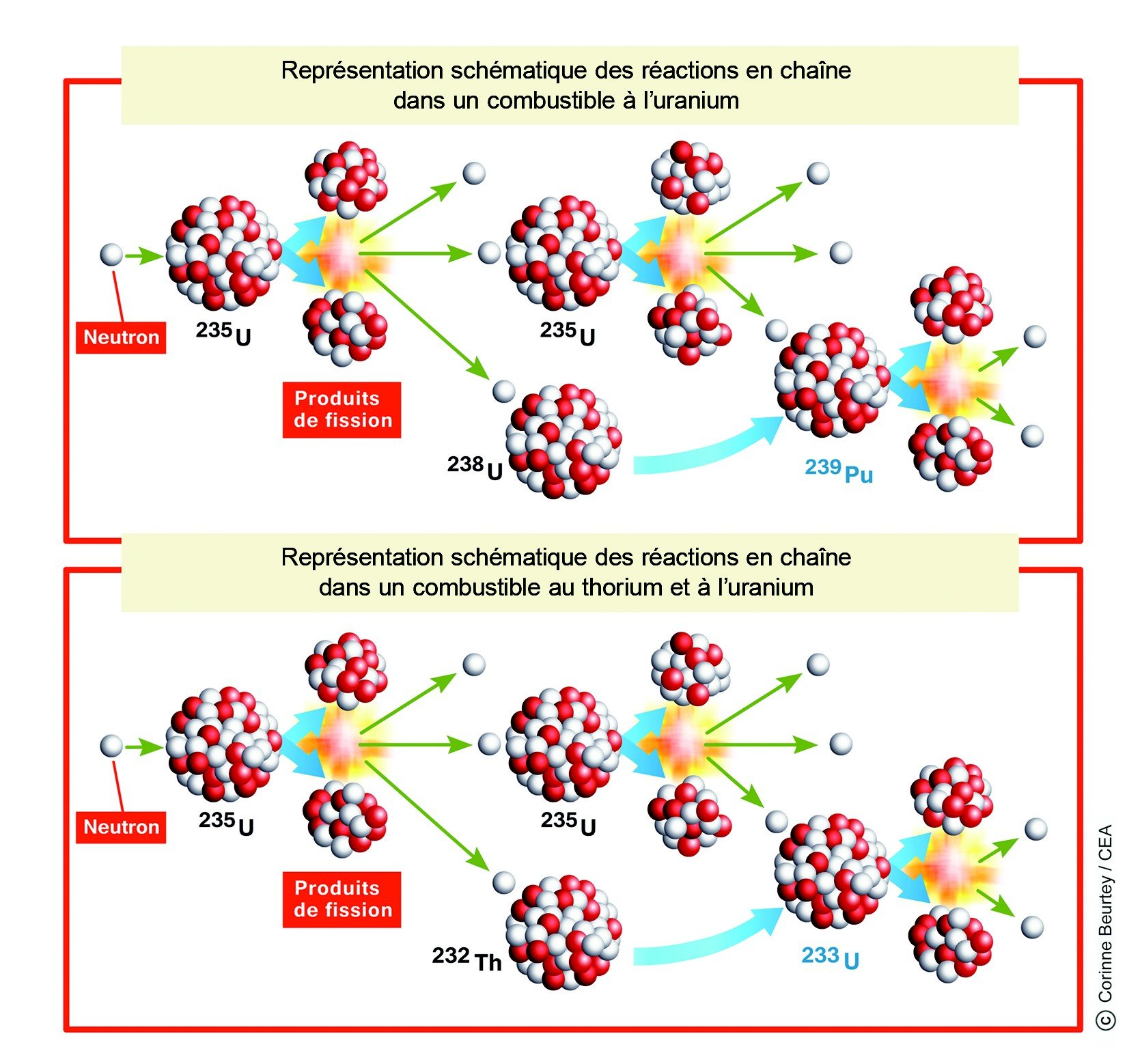
Le couple Th232-U233 permet, comme U238-Pu239, la surgénération avec des neutrons rapides.
Contraintes économiques
L'exploitation du thorium implique des méthodes d'extraction plus coûteuses que celle de l'uranium, selon l'AIEA(3). « La recherche, le développement et les essais d'installations nucléaires alimentées au thorium sont tout aussi coûteux en raison d'un manque d'expérience significative avec la prééminence historique du thorium et de l'uranium dans l'énergie nucléaire », souligne l'Agence.
Le retraitement des combustibles usés au thorium nécessite par ailleurs le développement, au niveau industriel, d’un procédé spécifique (procédé thorex), distinct de celui utilisé pour l’uranium, ajoute le CEA.
Le thorium dans le monde
Ressources estimées
La proportion de thorium dans la croûte terrestre est « de l'ordre de un cent-millième, c'est-à-dire qu'il est plus abondant que l'étain, l'arsenic et les métaux précieux. Il y en a deux fois moins que le plomb, quatre fois moins que le zinc, dix fois moins que le cuivre, mais il est de trois à quatre fois plus abondant que l'uranium », selon le CEA. L'AIEA évoque un même ratio entre la concentration estimée de thorium (10,5 parts par million) et celle d'uranium (3 ppm).
L'AIEA estimait les ressources mondiales de thorium à 6 355 000 tonnes à fin 2016. Ces ressources de thorium seraient principalement situées dans 7 pays selon les connaissances actuelles (par ordre d'importance)(4) :
- en Inde (846 000 tonnes, soit environ 13% des ressources mondiales) ;
- au Brésil (632 000 tonnes);
- en Australie (595 000 tonnes) ;
- aux États-Unis (595 000 tonnes) ;
- en Égypte (380 000 tonnes) ;
- en Turquie (374 000 tonnes);
- au Venezuela (300 000 tonnes).
Inde, Norvège, Chine...
L’Inde consacre actuellement un programme important de recherche pour l'utilisation du thorium dans des surgénérateurs à neutrons rapides, ce pays possédant également d’importantes ressources de ce minerai longtemps resté dans l’ombre de l’uranium (et de faibles ressources d'uranium par ailleurs).
La Chine a pour sa part annoncé à l'été 2021 l'achèvement d'un premier réacteur nucléaire expérimental au thorium, au milieu du désert de Gobi.
En Norvège, Thor Energy a réalisé une série d’essais avec du thorium dans le réacteur nucléaire de recherche de Halden (au sud-ouest de la Norvège), avant son arrêt en 2018.